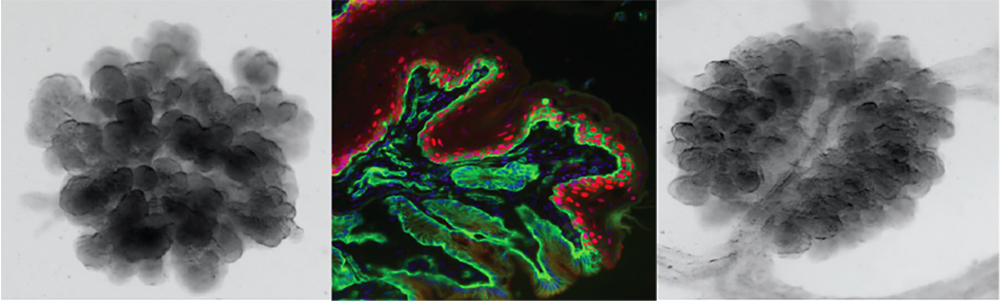
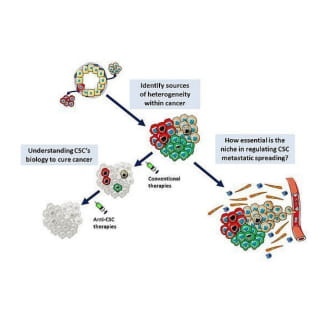
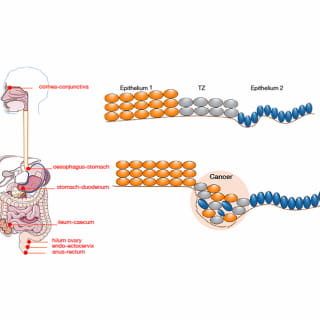
A genome-wide RNAi screen reveals essential therapeutic targets of breast cancer stem cells.
Arfaoui A, Rioualen C, Azzoni V, Pinna G, Finetti P, Wicinski J, Josselin E, Macario M, Castellano R, Léonard-Stumpf C, Bal A, Gros A, Lossy S, Kharrat M, Collette Y, Bertucci F, Birnbaum D, Douik H, Bidaut G, Charafe-Jauffret E, Ginestier C